你身邊有人罹患失智症嗎?失智症和其他破壞身體的疾病很不一樣,它攻陷和摧毀心智,使我們最愛的人變成陌生人。其中,有六到七成的失智症患者都患有阿茲海默症,2023 年 5 月,對抗阿茲海默症的護腦基因研究出爐,有機會打破幾乎束手無策的現狀,催生出治病的新藥和新策略。而且,這是 6000 人、跨越 30 多年用他們的人生教給我們的一堂課。
為什麼整個世紀阿茲海默症都沒藥醫?
1906年德國一位醫師阿茲海默(Alois Alzheimer)發表一個病例,這名女性患者在生前接受治療的期間答非所問、時間感混亂,也不知道自己身在何處,這種導致大腦病變的疾病後來就稱為阿茲海默症(Alzheimer’s disease)。
這位病患過世後,阿茲海默醫師解剖她的大腦,發現腦部嚴重萎縮,而且腦組織的切片經過銀染色後,可以看到布滿許多斑塊,神經細胞也扭曲變形,這兩種腦部的變化到現在還是診斷阿茲海默症的重要依據。
後來的科學家接棒研究,檢驗出這些斑塊是由一類叫做類澱粉蛋白質(amyloids)的不可溶蛋白質所形成,這些蛋白質會沉澱在神經細胞外面,部分研究者猜想這些斑塊或許是導致神經細胞活性衰減或死亡的兇手。而這些異常蛋白質跟食物裡的澱粉沒有關係,只是因為染色以後看起來和澱粉染色類似,澱粉的拉丁語是 amylum,所以早期的科學家就把它叫做類澱粉蛋白質 amyloid,一直延用到今天。
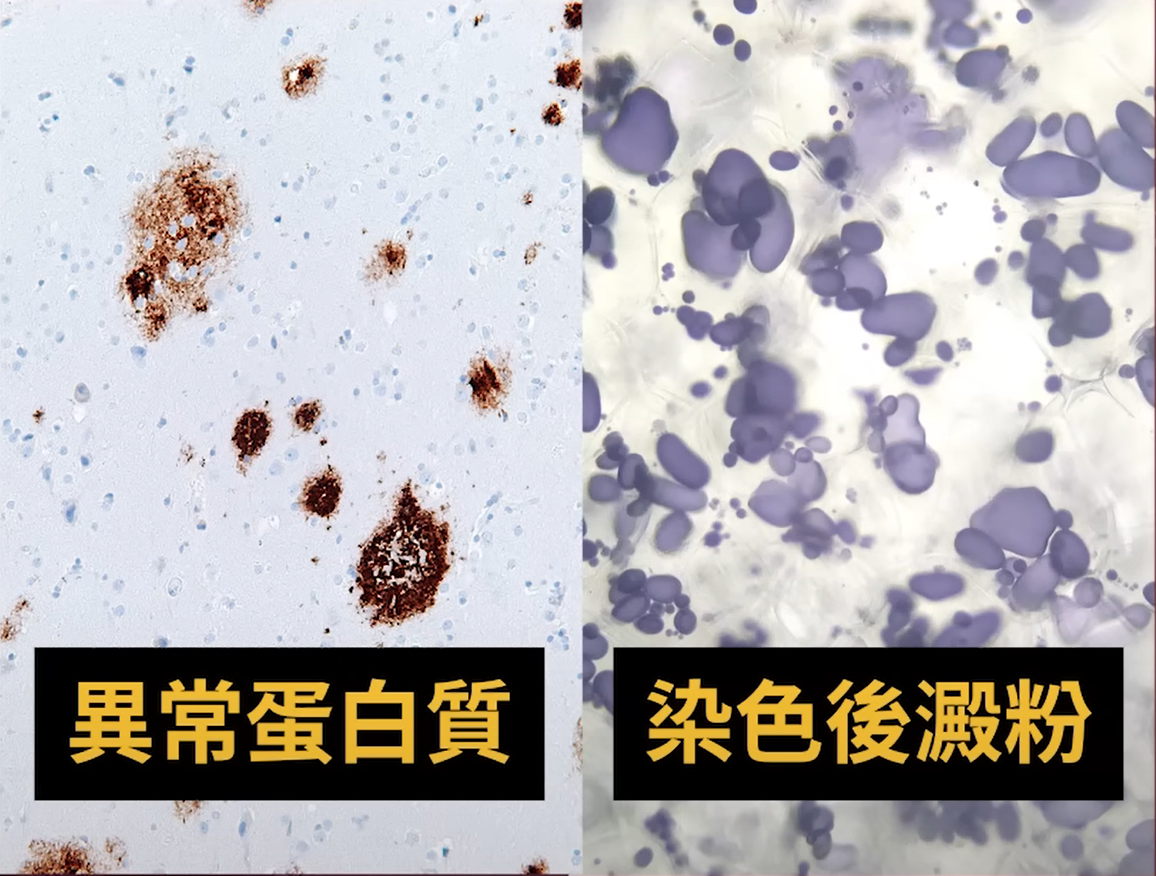 異常蛋白質染色以後看起來和澱粉染色類似。圖/PanSci YouTube
異常蛋白質染色以後看起來和澱粉染色類似。圖/PanSci YouTube神經細胞的扭曲變形則是因為神經細胞裡面冒出了大量的 Tau 蛋白質,這種蛋白質會在細胞內部聚集成雜亂糾結的纖維狀結構,也可能因此造成神經細胞沒辦法正常運作。
抓到大腦異狀的可疑元凶了,離找到解藥就不遠了吧?沒想到焦急的病患和家人們這一等,就等了快要 90 年。
第一個阿茲海默症的藥一直到 1993 年才推出,而且只能延緩心智瓦解的速度,沒辦法逆轉病程。1993 到 2003 年之間,一共有 5 種藥上市,其中 4 種的功效是提高神經傳導物質乙醯膽鹼的濃度,使神經訊號能順利傳送;另一種藥作用在神經細胞膜上的 NMDA 受體(N-methyl-D-aspartate receptor),這種受體分布在腦部多個區域,可以接收神經訊號,和認知學習有關。打個比方,這些藥都像是給瀕臨油盡燈枯的腦神經細胞打強心針,再盡可能多傳遞一些訊號,只能暫時減輕症狀,沒辦法解除病因。
目前全球失智症患者估計已經超過五千五百萬人,估計 2050 年時會膨脹到將近一億四千萬人;臺灣更是現在進行式,推估 80 歲以上每 5 個人就有 1 個人失智。一個影響如此之大的疾病,卻只有少得可憐的解方。綜觀整部醫療史,這種山窮水盡的情況其實很少見,其他的病再怎樣難纏,或多或少總可以想出一些辦法,就算是萬病之王癌症,人類還是不斷做出新藥、新療法,不會落到這種兩手一攤無計可施的地步。
 臺灣五歲分年齡層失智症盛行率。圖/台灣失智症協會
臺灣五歲分年齡層失智症盛行率。圖/台灣失智症協會2003 年以後又是一大段空白,到了 2021 年——距離發現阿茲海默症已經有 115 年之久——終於有新藥 Aducanumab 問世,它是第一種直接針對可能病因的藥物,鎖定的目標是清除類澱粉蛋白質。
爭議藥物強行通關,FDA委員憤而辭職
然而這款藥飽受爭議。大致來說,它最大的問題是雖然能減少類澱粉斑塊,但是只有部分受試患者的認知功能稍有改善。當時美國食品及藥物管理局(FDA)諮詢委員會的 11 名委員中 1 人棄權、10 個人投下反對票,可見得專家並不認同這款藥達到上市標準,但是 FDA 還是在病患人數多、有迫切醫療需求等等考量下強行核准過關。事後陸續有 3 名專家憤而辭職,掀起醫界不小的波瀾。
2023 年 1 月,第二種新藥 Lecanemab 推出,治療過程中可以把認知功能退化速度減少約四分之一;5 月上旬,第三種藥 Donanemab 公布第三期人體臨床試驗結果,減少認知退化速度約三分之一。兩種藥也都針對類澱粉斑塊,療效比第一種藥 Aducanumab 好了不少,但是使用上有限制,例如 Lecanemab 建議在疾病早期使用,效果可能比較好,然而很多阿茲海默症患者確診時已經是中晚期。兩種藥也有副作用,例如用藥後部分患者發生腦水腫或腦出血。
換句話說,現在寥寥無幾的藥都還有無法忽視的缺陷。找藥已經找到焦頭爛額的科學家,靈光一閃,另闢蹊徑從基因下手。而且,真的在陰霾中找到了一線亮光。
害腦基因 VS. 護腦基因,腦部小宇宙裡的戰爭
過去兩三個世代的科學家費盡心思,上山下海去搜索和阿茲海默症罹病風險相關的基因,他們決定直球對決:想辦法抑制或清除掉致病基因產生的壞東西,大腦自然就沒事了。
比如說,第一型早老素(PSEN1)、第二型早老素(PSEN2),以及 APOE 脂蛋白(Apolipoprotein E)基因等等。早老素顧名思義,被認為和腦神經功能衰退相關;APOE 則是和人體代謝膽固醇及三酸甘油酯有關,也會影響腦部類澱粉蛋白質的沉積過程。
有會傷害大腦的基因,那有沒有能保護大腦的基因呢?
但是也有科學家偏要和別人逆向,他們問的問題很簡單:既然有會毒害大腦的基因,那有沒有能保護大腦的基因呢?他們認為,只要弄清楚這些基因是用什麼方式為腦細胞穿上金鐘罩鐵布衫,人類就可以效仿了。
但是這種研究非常困難。原因是如果要找壞基因,可以藉由比對病人和健康人的 DNA,先勾勒出一個模糊的輪廓。就好像拿癌細胞和健康細胞來互相比較,可以挖到深埋在 DNA 裡的致癌基因。但是要找護腦基因,卻沒有對照組可以當成參考的基準點。也因為這個主要障礙,這類研究推進得相當龜速。
為什麼沒有對照組呢?因為最理想的受測者必須滿足三項條件。第一,他體內要攜帶能保護腦的基因,雖然科學家這時候還不知道這些基因是什麼;第二,他同時也帶有會傷害腦的基因;還有關鍵的第三點,那就是要可以觀察到護腦基因發功,壓過傷腦基因的破壞力道。
天啊,這也太困難了!不過科學家找到了理想的試驗對象,或許更精確的形容詞是,終於讓他們「等」到了。
尋找阿茲海默症致病基因——阿茲海默症家族
在南美洲哥倫比亞,有一個被早發型阿茲海默症魔咒纏身的大家族,人數約有 6 千人,其中許多人通常在 40 到 50 歲間就發病,遠比一般人早,病情惡化速度也更快。科學家追蹤這個家族 30 多年,鑑別出和腦部退化相關的多個遺傳因素。
2023 年 5 月,研究團隊在《Nature Medicine》發表成果,他們分析了大約一千兩百位帶有早發型致病基因的家族成員,從中找到一名特殊個案,這個男性首次接受認知功能測試的時候是 67 歲,已經超過發病年齡中位數 20 多年,但是卻只有輕度的認知障礙,沒有惡化成失智。
之後,科學家掃描這個人的大腦,發現腦部堆積大量的類澱粉斑塊,還有 Tau 蛋白質造成的神經細胞纖維糾結,簡單來說,他的大腦就像一個嚴重失智病人的腦。不過,其中有一塊名叫內嗅皮質(entorhinal cortex)的腦區,只有少少的 Tau 蛋白質。
內嗅皮質緊貼著掌管記憶形成過程的海馬迴(hippocampus),它的角色有點像海馬迴的守門人,能把遠處腦區傳來的電訊號接力送進海馬迴,先前已知內嗅皮質和記憶及空間定位能力有關。
2014 年諾貝爾生醫獎得主歐基輔和穆瑟夫婦,因為發現動物利用腦中一組排列成六角形網格狀的特殊細胞來記住地圖和認路,因而獲得殊榮,網格細胞就是位在內嗅皮質。阿茲海默症患者的內嗅皮質通常在疾病早期就遭到破壞,因此導致頻繁迷路、出得了門回不了家的症狀。或許我們該幫索隆檢查一下內嗅皮質?
 常常迷路的索隆。圖/tenor
常常迷路的索隆。圖/tenor研究團隊進一步分析這個男性的基因,發現他有一個稱為 RELN 的基因發生突變。RELN 基因已知和思覺失調症、躁鬱症等腦部變化有關聯,但科學家以往對這個基因和阿茲海默症的關聯了解得不多。
RELN 基因和阿茲海默症的關聯
為了瞭解這種突變會觸發什麼後續效果,研究者改造小鼠的基因,試驗結果發現,突變 RELN 基因轉譯出來的蛋白質,會促使 Tau 蛋白質發生化學修飾,降低了某些腦區裡 Tau 蛋白質聚集形成纖維糾結的能力。
這項研究其實是史上第二例基因突變大幅延緩早發型阿茲海默症病程的報告,第一例是同一個家族的一位女性,2019 年發表在《Nature Medicine》,她比同家族人晚了將近 30 年才發病,不過她發生突變的地方是在 APOE 基因,突變後 APOE 脂蛋白的致病力減弱,比較難以造成腦部病變。
阿茲海默的新假設與新挑戰
這兩份研究報告帶出了一個假設,以及一個挑戰。新的假設是,用人為方式加強 RELN 的護腦效果,或是削弱 APOE 的傷腦能力,對於開發新藥和新療法來說可能是更好的目標。
不過,持平來說,目前這類護腦基因突變僅僅發現兩例,還太少了,只能用試驗結果建立假說,也不能確定是不是適用於所有患者,必須累積更多調查和試驗數據才能判斷。
提出的新挑戰則是,現在 FDA 核准的藥物都是鎖定類澱粉蛋白質為目標,還有一大堆同類的藥正在燒鈔票試驗中,但是新研究對於類澱粉斑塊致病假說是一記強而有力的警鐘。或許 Tau 蛋白質的角色一直被誤解了,它才是真正的幕後黑手?又或許根本不需要保護整個腦,只要想辦法保住關鍵腦區或必要的神經元通道,就可以對抗阿茲海默症?這些問題都是接下來研究的重點。
腦真的是類澱粉蛋白質殺的?阿茲海默症研究風向轉變中
類澱粉蛋白質是主要致病元兇的說法在近幾年已經受到不少質疑。原因有好幾個,概略來說,主因是科學家陸陸續續看到一些當事人大腦裡有類澱粉斑塊沉積,但是心智沒有明顯受影響的案例;還有,長久以來全球許多研究團隊把類澱粉蛋白質當作開發藥物的目標,結果失敗率幾乎是 100%,也讓人對這個假說起疑。
就在 2022 年,阿茲海默症醫療史上一樁惡名昭彰的醜聞爆發,更把致病原因的爭議推上最高點。
事件導火線是一位神經科學家揭露 2006 年發表在《Nature》的一篇阿茲海默症經典論文涉嫌造假,這篇報告以及它後續的研究,提出某個類型的類澱粉蛋白質可能導致阿茲海默症的看法。2022 年 7 月《Science》刊出長篇報導,指出科學界調查認為有數百張論文圖片疑似有問題。
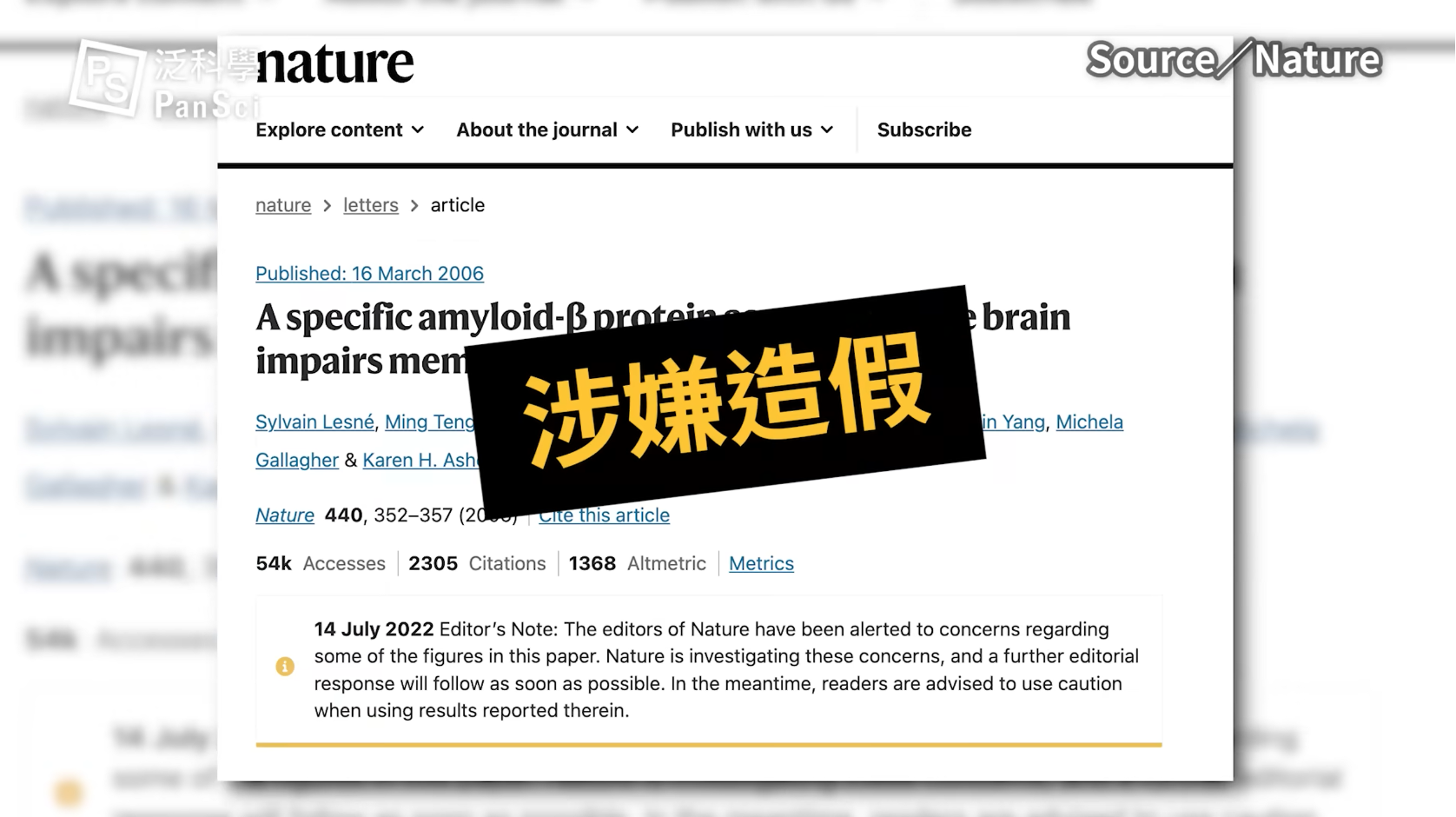 2006 年發表在《Nature》的一篇阿茲海默症經典論文涉嫌造假,調查認為有數百張論文圖片疑似有問題。圖/PanSci YouTube
2006 年發表在《Nature》的一篇阿茲海默症經典論文涉嫌造假,調查認為有數百張論文圖片疑似有問題。圖/PanSci YouTube這把火最直接燒出來的問題是,會不會整整十六年來大家都被誤導了?白白浪費了大批科學家的時間,連帶燒掉幾千萬甚至幾億美元。這裡我們沒辦法再多講細節,如果你想更詳細瞭解這場「阿茲海默之亂」和後續影響,想知道研發阿茲海默藥物的百年崎嶇路和未來進程的更多新知,或是想跟上失智症的其他最新研究,歡迎加入我們的頻道會員來投票喔!
不過,這並不是說類澱粉斑塊假說就此被一竿子打翻,畢竟很多患者大腦有明確的斑塊沉積是事實,而且醜聞裡牽涉到的只是類澱粉蛋白質之中的特定類型;再加上 2023 年針對類澱粉斑塊的 Lecanemab 和 Donanemab 兩款新藥的確有療效,也是有力的佐證。
目前生物醫學界的看法,逐漸轉向認為阿茲海默症很可能不是單一種疾病,而是應該再切分出多種亞型,類澱粉蛋白質斑塊是部分患者的病因但不是全部。打個比方,就好像同樣是肺癌,按照基因差異和疾病進程不同,醫師和科學家可以把患者再分成多個小群,每一群都有相對更適合的療法。
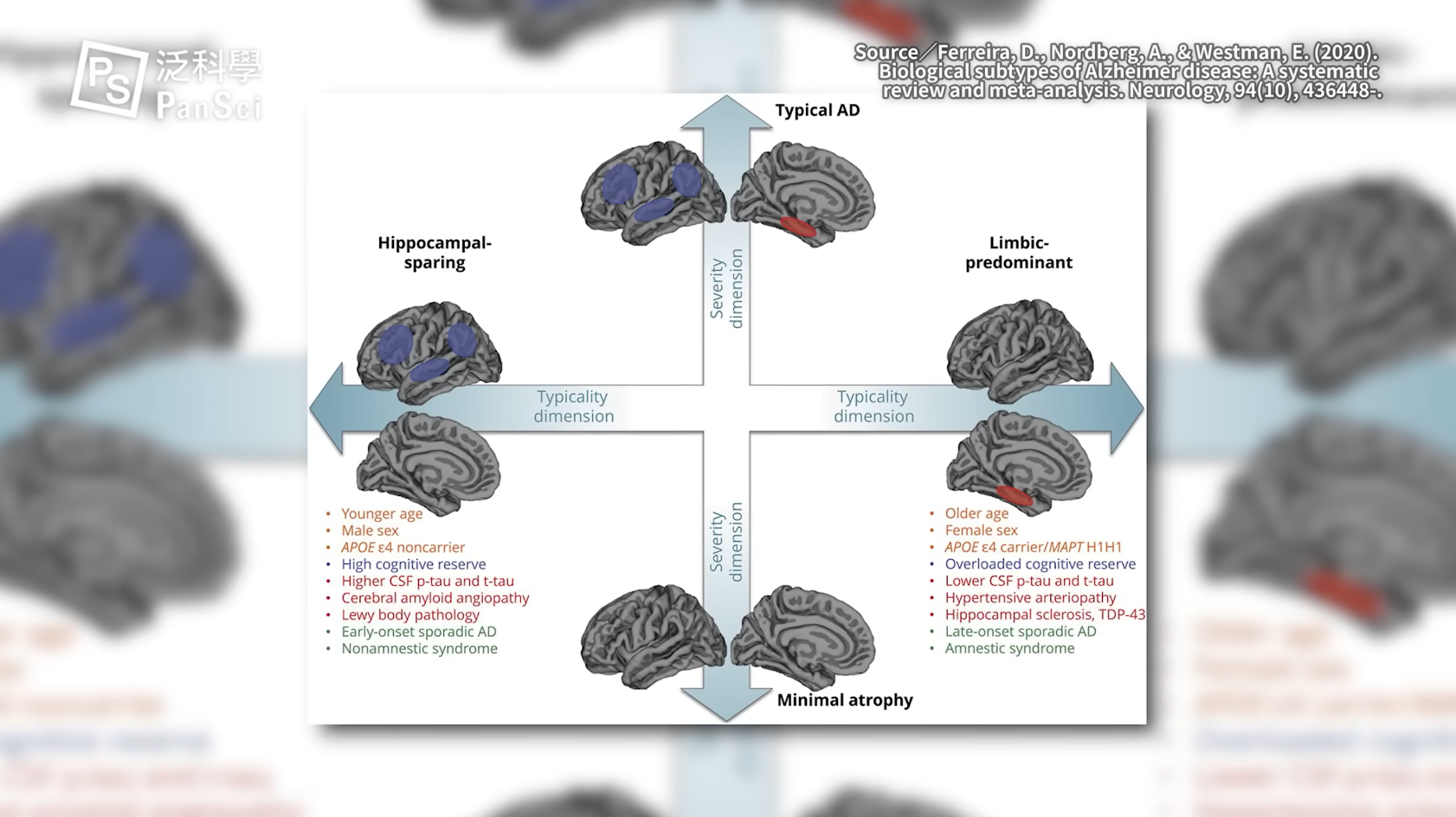 阿茲海默症很可能不是單一種疾病,而是應該再切分出多種亞型。圖/PanSci YouTube
阿茲海默症很可能不是單一種疾病,而是應該再切分出多種亞型。圖/PanSci YouTube舉例來說,前面說到的從阿茲海默症家族發現的傷腦和護腦基因,以及關鍵腦區有沒有受損,或許就有機會成為打開分型治療之門的幾把鑰匙。
如果這個多亞型的新觀點成立的話,那麼要怎麼樣為患者分型?有哪些生物標記可以用?每種亞型要怎麼治療?這些一連串問題勢必會變成接下來研究的重點,我們也可以想像得到,阿茲海默症的醫療即將出現百花齊放的局面,不過呢,這又是另一個故事了。如果你身邊有人也對這個議題好奇,歡迎分享給他,如果你就是阿茲海默症的患者跟照顧者,在此跟你說聲辛苦了。
歡迎訂閱 Pansci Youtube 頻道 獲取更多深入淺出的科學知識!




 ufabet
มีเกมให้เลือกเล่นมากมาย: เกมเดิมพันหลากหลาย ครบทุกค่ายดัง
ufabet
มีเกมให้เลือกเล่นมากมาย: เกมเดิมพันหลากหลาย ครบทุกค่ายดัง


