编译 | 曾全晨
审稿 | 王建民
今天为大家介绍的是来自Falk W. Lohoff团队的一篇论文。

人类衰老是一个受多种因素影响的多方面过程。一些个体可能会遭受慢性健康问题和疾病并早逝,而其他人可能在相对健康的状态下达到老年。了解这种变异的基础因素对于制定公共卫生干预和改善健康衰老的治疗方法非常重要。全基因组关联研究(GWAS)已经开始使用单一表型方法,包括极端长寿、健康寿命和亲代寿命,来识别与衰老相关的位点。然而,这些单一方法未能考虑到这些特征或其他与衰老相关的特征之间共享的遗传学如表观遗传学年龄加速(EAA)和虚弱,这些因素可以进一步揭示人类衰老的广泛遗传结构,并为研究生存向纳入年龄相关结果的互补措施的转变提供信息,以改善健康衰老,即在老年阶段维持幸福、满意和充实感。在这里,作者将基因组结构方程模型应用于构建多变量衰老相关的GWAS(在此称为“mvAge”),以识别广泛影响健康衰老过程的新遗传变异。
研究总览
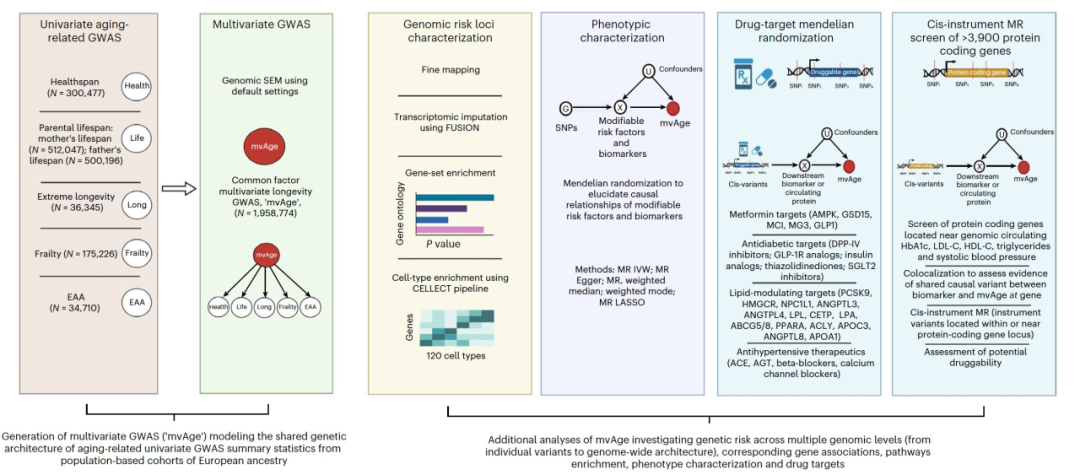
图 1
研究的数据来源、分析流程和方法概述如图1所示。衰弱和表观年龄加速度(EAA)的单变量输入GWAS被逆向编码,以使它们的效应与健康寿命和极端长寿之间具有正相关关系。
结构方程模型
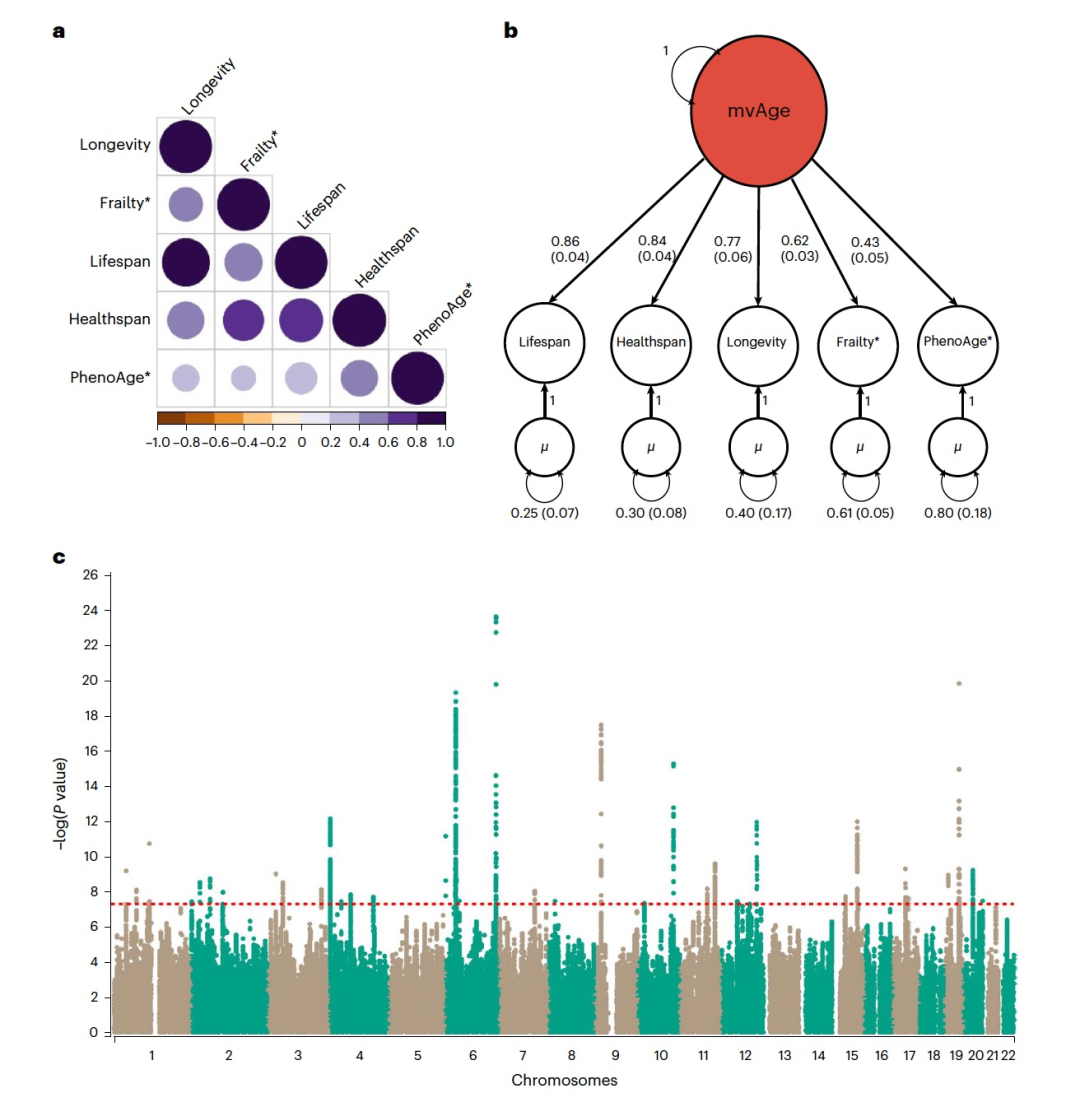
图 2
Linkage disequilibrium(LD)分数回归表明,代表健康寿命、衰弱、特殊长寿、父母寿命和表观年龄加速度的五个单变量输入GWAS之间存在正相关关系(衰弱和表观年龄加速度进行了反向编码)(图2)。作者进行了结构方程建模(SEM)来准备多变量GWAS。共同因子模型与五个输入GWAS之间的遗传协方差矩阵的拟合效果很好(图2),表明存在共享遗传因子mvAge的证据。
多变量遗传关联研究
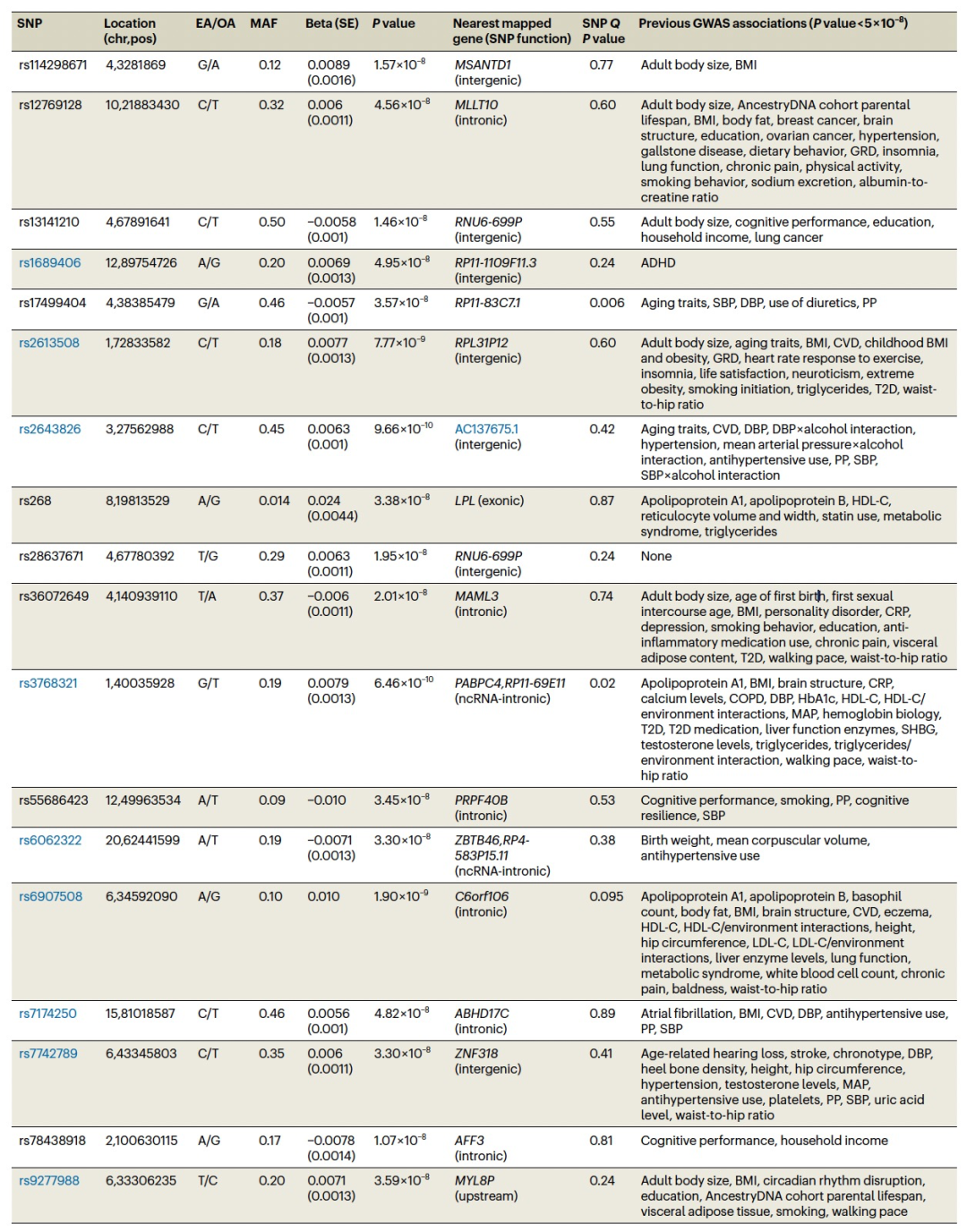
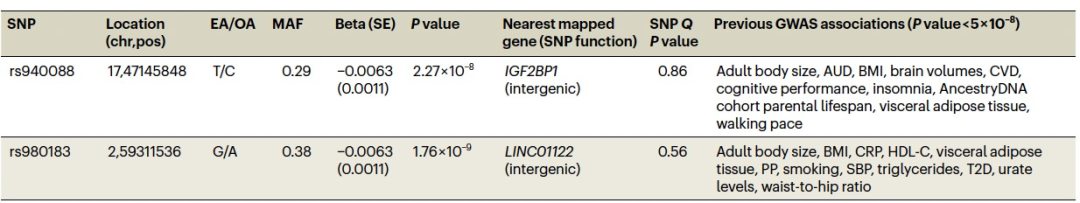
表 1
为了扩展SEM模型以包括个体变异,作者对单核苷酸多态性(SNP)水平的共享老化因子mvAge估计了6,793,898个关联。作者在38个基因组位点中确定了52个主要SNPs(图2)。与支撑mvAge的五个输入GWAS相比,其中20个SNPs是新的,这突显了基因组SEM的增强功效。新的mvAge主导SNPs是特征丰富的,如收缩压(SBP)、体质指数(BMI)、大脑形态和2型糖尿病(T2D)。在20个新的SNPs中,有11个主要SNP在以前全基因组关联研究中被确定,11个新的变种中有4个(rs12769128, rs17499404, rs2643826和rs9277988)与与老化相关的特征连接,而另外四个(rs114298671, rs1689046, rs78438918和rs6062322)没有与特定的老化表型连接;但是,它们与可能影响健康老化的重要因素相关联(例如,认知,BMI和高血压)(表1)。
精细定位
通过详细分析,作者发现了一些与特定基因位置紧密关联的标记。例如,在染色体1上找到了一个标记rs1230666,它位于MAGI3基因的一个段落里;在染色体6上注意到了rs12203592和rs9277988;染色体8上有一个标记rs268,它直接位于LPL基因中;在染色体19上找到了APOE基因位置的rs7412;最后,在染色体20上作者发现了rs1737896。作者绘制的图表清晰地展示了这些基因位置的显著性,证明了它们与某些遗传特征的关系(详情请见论文附录)。
转录组模拟
作者使用FUSION进行了一个基因水平的关联分析,来查看哪些基因与mvAge的遗传特征有关。作者找到了57个这样的基因,并对这些基因进行了深入的测试,包括共定位分析和FOCUS细分映射分析。在这57个显著的基因中,有18个与mvAge有可能的因果关系。这些“高信度”的基因关联包括CDKN2A, PTPN22, PHB1和VEGFA。CDKN2A和VEGFA的分数都是正数,意味着当这些基因的表达增加时,mvAge也增加。反之,PTPN22和PHB1的分数是负数,说明这两个基因表达的减少与mvAge的增加有关。
结论
作者利用最近发展的多变量基因组关联研究(multivariate GWAS)方法来阐明健康老化的广泛遗传基础。所鉴定的位点反映了与健康老化相关的基础性遗传特征,与当前老龄科学的研究方向一致,该方向侧重于系统层面的研究,旨在改善健康老化并减缓老化过程。作者进行了生物信息学分析,以确定可能的因果基因、细胞类型、生物标志物和可改变的风险因素。
参考资料
Rosoff, D.B., Mavromatis, L.A., Bell, A.S. et al. Multivariate genome-wide analysis of aging-related traits identifies novel loci and new drug targets for healthy aging. Nat Aging 3, 1020–1035 (2023).
https://doi.org/10.1038/s43587-023-00455-5




 ufabet
มีเกมให้เลือกเล่นมากมาย: เกมเดิมพันหลากหลาย ครบทุกค่ายดัง
ufabet
มีเกมให้เลือกเล่นมากมาย: เกมเดิมพันหลากหลาย ครบทุกค่ายดัง





